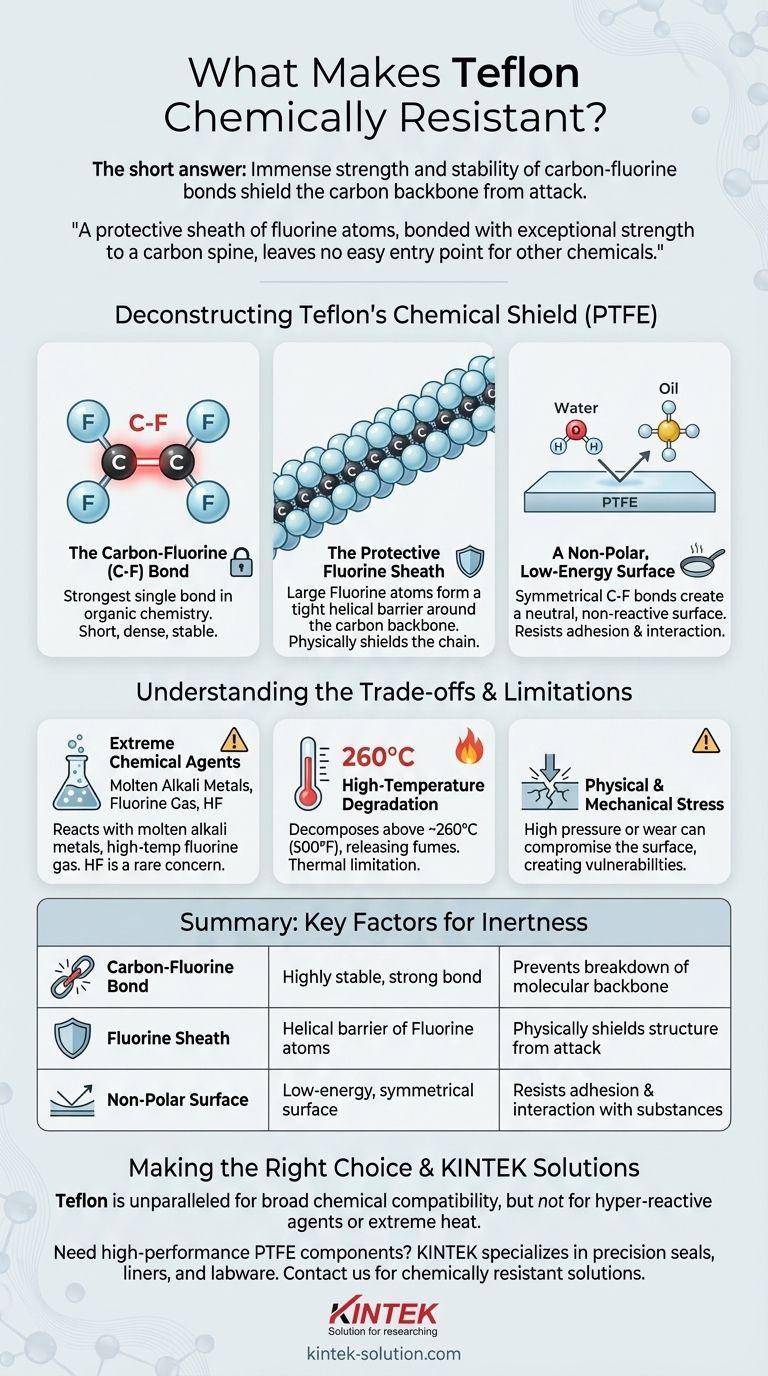
간단히 말해, 테플론의 놀라운 내화학성은 분자 구조를 이루는 탄소-불소 결합의 엄청난 강도와 안정성 때문입니다. 이 결합은 반응성이 극도로 낮은 표면을 만들어 거의 모든 산, 염기 및 용매의 공격으로부터 분자의 탄소 골격을 효과적으로 차폐합니다.
테플론의 비활성의 핵심 이유는 원자 구조에 있습니다. 매우 강한 힘으로 탄소 척추에 결합된 불소 원자의 보호 외피는 다른 화학 물질이 반응을 시작할 수 있는 쉬운 진입점을 남기지 않습니다.
테플론의 화학적 차폐 해부
테플론의 내성을 이해하려면 분자 수준에서 그 구조를 살펴봐야 합니다. 테플론은 가장 일반적으로 폴리테트라플루오로에틸렌(PTFE)인 고분자의 상표명입니다.
탄소-불소 결합
PTFE의 특징적인 요소는 탄소-불소(C-F) 결합입니다. 이 결합은 유기 화학에서 가장 강력한 단일 결합 중 하나입니다.
불소는 가장 전기음성도가 높은 원소로, 전자를 매우 강하게 끌어당깁니다. 이로 인해 탄소와 매우 짧고 밀도가 높으며 안정한 결합이 형성되어 끊기가 어렵습니다.
보호 불소 외피
PTFE 분자는 탄소 원자의 긴 사슬로 구성됩니다. 각 탄소 원자는 두 개의 불소 원자와 결합되어 있습니다.
이 불소 원자들은 결합된 탄소 원자보다 크기 때문에 탄소 골격 주위에 단단한 나선형 외피를 형성합니다. 이 물리적 장벽은 더 취약한 탄소 사슬을 화학적 공격으로부터 추가로 보호합니다.
비극성, 저에너지 표면
C-F 결합의 대칭적인 배열은 비극성 표면을 만듭니다. 이러한 전하 부재는 물과 같은 극성 용매나 기름과 같은 비극성 용매를 포함하여 다른 분자와 매우 약한 상호작용을 한다는 것을 의미합니다.
이러한 낮은 표면 에너지는 테플론이 논스틱(non-stick) 특성으로 알려진 이유이기도 합니다. 다른 물질이 "붙잡을" 것이 없기 때문입니다.

절충점 및 한계 이해
테플론은 내화학성이 뛰어나지만 무적은 아닙니다. 몇 가지 약점을 이해하는 것은 안전하고 효과적인 적용을 위해 중요합니다.
극한의 화학 물질
반응성이 높은 소수의 물질이 특정 조건에서 테플론을 공격할 수 있습니다. 여기에는 나트륨과 같은 용융 알칼리 금속과 고온 및 고압에서 원소 불소 가스와 같은 강력한 불소화제가 포함됩니다.
일부 자료에서는 불산(HF)이 특정 테플론 코팅 부품에 문제가 될 수 있다고 언급하는데, 이는 산 내성의 드문 예외입니다.
고온 분해
테플론의 내화학성은 물리적 무결성과 관련이 있습니다. 매우 높은 온도(일반적으로 PTFE의 경우 260°C 또는 500°F 이상)에서는 재료가 분해되기 시작합니다.
직접적인 화염은 분해를 일으켜 잠재적으로 유해한 증기를 방출할 수 있습니다. 이는 일반적인 화학 반응성 문제라기보다는 열적 한계입니다.
물리적 및 기계적 응력
가혹한 환경에서는 물리적 응력이 취약점을 만들 수 있습니다. 높은 압력이나 기계적 마모는 재료 표면을 손상시켜 공격적인 화학 물질이 고분자를 분해하기 시작할 수 있는 부위를 만들 수 있습니다.
귀하의 응용 분야에 맞는 올바른 선택
재료를 선택하려면 작동 환경에 특성을 맞춰야 합니다.
- 주요 초점이 광범위한 화학적 호환성인 경우: 테플론은 실험실 또는 산업 환경에서 대부분의 일반적이고 공격적인 산, 염기 및 유기 용매를 취급하는 데 비할 데 없는 선택입니다.
- 주요 초점이 고온 공정인 경우: 테플론 변형(예: PTFE, PFA, FEP)의 특정 온도 정격을 확인하고 분해점보다 훨씬 낮은 온도를 유지해야 합니다.
- 주요 초점이 틈새의 초고반응성 화학 물질과 관련된 경우: 용융 알칼리 금속이나 고압 불소 가스와 관련된 응용 분야의 경우 테플론은 적합한 재료가 아니므로 대안을 찾아야 합니다.
궁극적으로 테플론의 화학적 비활성은 독특하고 견고한 분자 설계의 직접적인 결과입니다.
요약표:
| 핵심 요소 | 설명 | 내화학성에 미치는 영향 |
|---|---|---|
| 탄소-불소 결합 | 유기 화학에서 가장 강력한 결합 중 하나이며 매우 안정적입니다. | 대부분의 화학 반응이 분자 골격을 파괴하는 것을 방지합니다. |
| 불소 외피 | 불소 원자가 탄소 사슬 주위에 보호 나선형 장벽을 형성합니다. | 구조를 화학적 공격으로부터 물리적으로 차폐합니다. |
| 비극성 표면 | 대칭적인 C-F 결합은 저에너지의 비반응성 표면을 만듭니다. | 극성 및 비극성 물질과의 부착 및 상호작용에 저항합니다. |
까다로운 응용 분야를 위한 고성능 PTFE 부품이 필요하십니까? KINTEK은 반도체, 의료, 실험실 및 산업 분야를 위한 정밀 PTFE 씰, 라이너 및 실험실 기구 제조를 전문으로 합니다. 프로토타입부터 대량 주문까지 맞춤 제작 서비스를 통해 정확한 요구 사항에 맞는 내화학성 솔루션을 얻을 수 있도록 보장합니다. 지금 바로 문의하여 당사의 PTFE 전문 지식이 공정 신뢰성과 안전성을 어떻게 향상시킬 수 있는지 논의하십시오!
시각적 가이드
관련 제품
- 맞춤형 PTFE 여과 시스템 내산성 고순도 반도체 등급 화학 처리 필터
- 화학 저장 드럼 및 유체 이송 시스템용 고� 내부식성 PTFE 수전 폴리테트라플루오로에틸렌 밸브, 맞춤형 산업용 등급
- PTFE PFA 진공 여과 시스템 내부식성 맞춤형 방파성 실험실 장비
- PFA 밸브 연결과 일체형 체판을 갖춘 PTFE 내부식 필터
- 고온 내화학성 50ml PTFE 주사기, 추적 분석용 나사형 실링 커스텀 테플론 인젝터